化学分子イメージング
Chemical Imaging Techniques
TEL 06-6879-7924
FAX 06-6879-7875
概要
ケミカルバイオロジーは化学を用いた生物学研究を行う新しい研究分野であり近年注目を集めています。我々は、細胞内や動物体内の蛋白質の動態や酵素反応を蛍光やMRIによって可視化する化学プローブの開発に取り組んでいます(Figure 1, Figure 2)。これらの化学プローブを用い、生きたまま細胞や動物における生体分子の働きを調べることで、新たな生命機能の解明につながる多くの情報が得られることが期待できます。
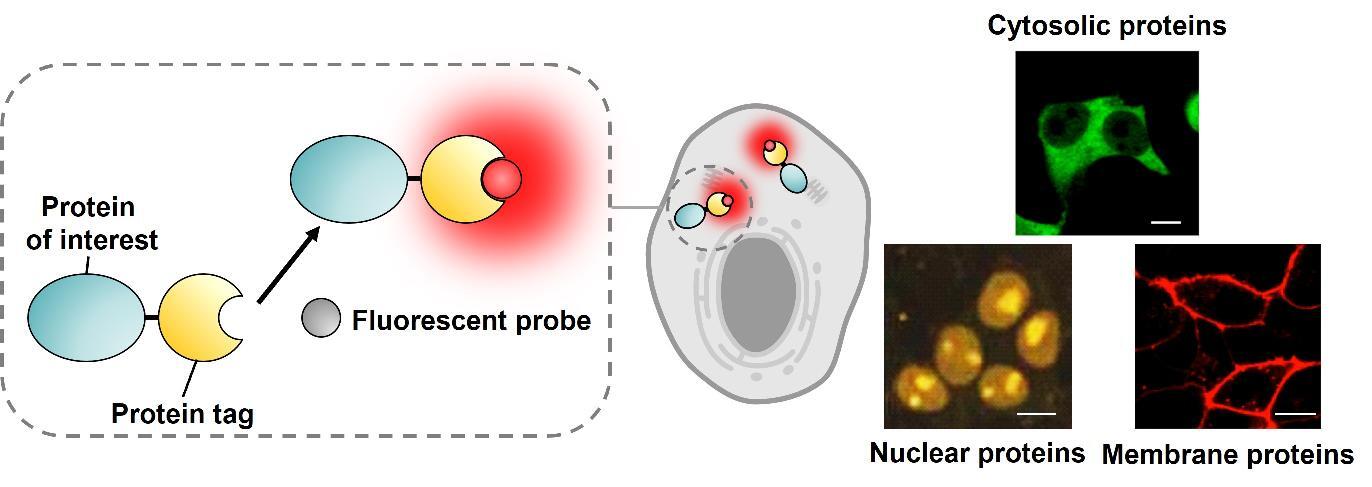
Figure 1. Fluorescent probes for live-cell imaging of proteins.
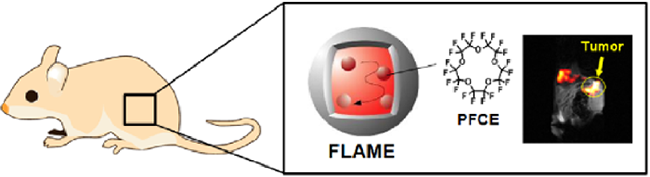
主任研究者
菊地 和也 教授

研究内容
生細胞内・個体内の生体分子を可視化するプローブ分子のデザイン・合成・生物応用
学歴
| 1984.4 | 東京大学教養学部理科II類入学 |
|---|---|
| 1986.4 | 東京大学薬学部進学 |
| 1988.3 | 東京大学薬学部卒業 |
| 1988.4 | 東京大学大学院薬学系研究科修士課程入学 |
| 1990.3 | 東京大学大学院薬学系研究科修士課程卒業 |
職歴
| 1990.4 | (株)武田薬品工業入社 |
|---|---|
| 1990.9 | (株)武田薬品工業退職 |
| 1990.10 | 東京大学大学院薬学系研究科大学院研究生 |
| 1991.4 | 東京大学大学院薬学系研究科博士課程入学 |
| 1994.3 | 東京大学大学院薬学系研究科博士課程卒業 |
| 1994.4 | 日本学術振興会博士特別研究員 |
| 1994.7 | カリフォルニア大学サンディエゴ校博士研究員 (化学及び生化学科・薬理学科Roger Y. Tsien教授) |
| 1995.7 | スクリプス研究所博士研究員(化学科Donald Hilvert教授) |
| 1997.1 | 東京大学大学院薬学系研究科助手 |
| 2000.12 | 東京大学大学院薬学系研究科助教授 |
| 2001.12 | 科学技術振興事業団「さきがけ研究21」「タイムシグナルと制御」研究領域 研究員 兼任 (-2005.3) |
| 2005.7 | 大阪大学大学院工学研究科生命先端工学専攻教授 |
| 2009.8 | 大阪大学免疫学フロンティア研究センター教授(兼任) |
受賞・表彰
| 2013.2 | 第29回(平成24年度)井上学術賞受賞 受賞題目:「化学プローブのデザイン・合成による分子イメージング」 |
|---|---|
| 2012.3 | 第29回(平成23年度)日本化学会学術賞受賞 受賞題目:「化学スイッチ機能を有した分子イメージプローブの合成と生物学への応用」 |
| 2011.7 | 平成23年度 大阪大学功績賞受賞 |
| 2010.3 | 第6回(平成21年度)日本学術振興会賞受賞 受賞題目:「生体内分子を可視化する化学プローブのデザイン・合成・生物応用」 |
| 2008.12 | Royal Society of Chemistry(英国王立化学協会) Emerging Investigator Award 受賞題目:"Design, Synthesis and Biological Application of Chemical Sensor Molecules Which Convert Biological Signals to Chemical Output" |
| 2008.11 | 第22回日本IBM科学賞受賞 受賞題目:「生体内分子を可視化する化学プローブのデザイン・合成・生物応用」 |
| 2004.11 | (社)日本バイオイメージング学会 平成16年度研究奨励賞受賞 受賞題目:"可視化プローブのデザイン・合成によるバイオイメージング" |
| 2002.5 | (財)富山県ひとづくり財団 平成14年度とやま賞受賞 受賞題目:"生細胞可視化プローブのデザイン・合成・生物応用" |
| 2002.3 | (社)日本薬学会 平成14年度奨励賞受賞 受賞題目:"生細胞蛍光プローブのデザイン・合成とその応用による可視化解析" |
| 2001.9 | (社)日本化学会生体機能関連化学部会 部会講演賞受賞 受賞題目:"新規亜鉛イオン蛍光センサー分子のデザイン・合成と生細胞可視化解析" |
メンバー
- 菊地 和也 教授
kkikuchimls.eng.osaka-u.ac.jp
業績
論文
- H. Maeda, T. Kowada, J. Kikuta, M. Furuya, M. Shirazaki, S. Mizukami, M. Ishii, & K. Kikuchi, ''Real-time intravital imaging of pH variation associated with osteoclast activity'', Nat. Chem. Biol., 12, 579-585 (2016)
- S. Hirayama, Y. Hori, Z. Benedek, T. Suzuki, & K. Kikuchi, ''Fluorogenic probes reveal a role of GLUT4 N-glycosylation in intracellular trafficking'', Nat. Chem. Biol., 12, 853-859 (2016)
- Y. Hori, S. Hirayama, M. Sato, & K. Kikuchi, ''Redesign of a Fluorogenic Labeling System to Improve Surface Charge, Brightness, and Binding Kinetics for Imaging the Functional Localization of Bromodomains'', Angew. Chem. Int. Ed., 54, 14368-14371 (2015)
- T. Nakamura, H. Matsushita, F. Sugihara, Y. Yoshioka, S. Mizukami, & K. Kikuchi, ''Activatable 19F MRI Nanoparticle Probes for the Detection of Reducing Environments'', Angew. Chem. Int. Ed., 54, 1007-1010 (2015)
- Z. Zeng, S. Mizukami, K. Fujita, & K. Kikuchi, ''An Enzyme-Responsive Metal-Enhanced Near-Infrared Fluorescence Sensor Based on Functionalized Gold Nanoparticles'', Chem. Sci., 6, 4934-4939 (2015)
- T. Nakamura, F. Sugihara, H. Matsushita, Y. Yoshioka, S. Mizukami, & K. Kikuchi, ''Mesoporous Silica Nanoparticles for 19F Magnetic Resonance Imaging, Fluorescence Imaging, and Drug Delivery'', Chem. Sci., 6, 1986-1990 (2015)
- H. Matsushita, S. Mizukami, F. Sugihara, Y. Nakanishi, Y. Yoshioka & K. Kikuchi, “Multifunctional Core-shell Silica Nanoparticles for Highly Sensitive 19F MRI”, Angew. Chem. Int. Ed., 53, 1008-1011 (2014).
- S. Okada, S. Mizukami, T. Sakata, Y. Matsumura, Y. Yoshioka, and K. Kikuchi, ''Ratiometric MRI Sensors Based on Core-Shell Nanoparticles for Quantitative pH Imaging'', Adv. Mater., 26, 2989-2992 (2014)
- Y. Hori, T. Norinobu, M. Sato, K. Arita, S. Shirakawa & K. Kikuchi, “Development of Fluorogenic Probes for Quick No-Wash Live-Cell Imaging of Intracellular Proteins”, J. Am. Chem. Soc., 135, 12360–12365 (2013).
- Y. Hori, K. Nakaki, M. Sato, S. Mizukami & K. Kikuchi, “Development of Protein Labeling Probes with Redesigned Fluorogenic Switch Based on Intramolecular Association and No-wash Live-cell Imaging”, Angew. Chem. Int. Ed., 51, 5611-5614 (2012).
- S. Mizukami, S. Watanabe, Y. Akimoto & K. Kikuchi, “No-Wash Protein Labeling with Designed Fluorogenic Probes and Application to Real-Time Pulse-Chase Analysis”, J. Am. Chem. Soc., 134, 1623-1629 (2012).
- R. Baba, Y. Hori, S. Mizukami & *K. Kikuchi, “Development of Fluorogenic Probe with Transesterification Switch for Detection of Histone Deacetylase Activity”, J. Am. Chem. Soc., 134, 14310-14313 (2012).
- T. Kowada, J. Kikuta, A. Kubo, M. Ishii, H. Maeda, S. Mizukami & K. Kikuchi, “In Vivo Fluorescence Imaging of Bone-Resorbing Osteoclasts”, J. Am. Chem. Soc., 133, 17772-17776 (2011)
- S. Mizukami, T. Yamamoto, A. Yoshimura, S. Watanabe & K. Kikuchi, “Covalent Protein Labeling with a Lanthanide Complex and its Application to Photoluminescence Lifetime-based Multicolor Bioimaging”, Angew. Chem. Int. Ed., 50, 8750-8752 (2011).
- S. Mizukami, M. Hosoda, T. Satake, S. Okada, Y. Hori, T. Furuta & K. Kikuchi, “Photocontrolled Compound Release System Using Caged Antimicrobial Peptide”, J. Am. Chem. Soc., 132, 9524-9525 (2010).
- S. Mizukami, R. Takikawa, F. Sugihara, M. Shirakawa & K. Kikuchi, “Dual Functional Probe to Detect Protease Activity for Fluorescence Measurement and 19F MRI”, Angew. Chem. Int. Ed., 48, 3641-3643 (2009).
- Y. Hori, H. Ueno, S. Mizukami & K. Kikuchi, “Photoactive Yellow Protein-Based Protein Labeling System with Turn-on Fluorescence Intensity”, J. Am. Chem. Soc., 131, 16610-16611 (2009).
- S. Mizukami, S. Watanabe, Y. Hori & K. Kikuchi, “Covalent Protein Labeling Based on Non-catalytic -Lactamase and a Designed FRET Substrate”, J. Am. Chem. Soc., 131, 5016-5017 (2009)
- S. Mizukami, R. Takikawa, F. Sugihara, Y. Hori, H. Tochio, M. Wälchli, M. Shirakawa & K. Kikuchi, “Paramagnetic Relaxation-based 19F MRI Probe to Detect Protease Activity”, J. Am. Chem. Soc., 130, 794-795 (2008).
- S. Mizukami, K. Tonai, M. Kaneko & K. Kikuchi, “Lanthanide-based Protease Activity Sensors for Time-resolved Fluorescence Measurements”, J. Am. Chem. Soc., 130, 14376-14377 (2008).
