皮膚アレルギー
生体防御
Cutaneous Allergy and Host Defense
TEL 06-6879-4963
概要
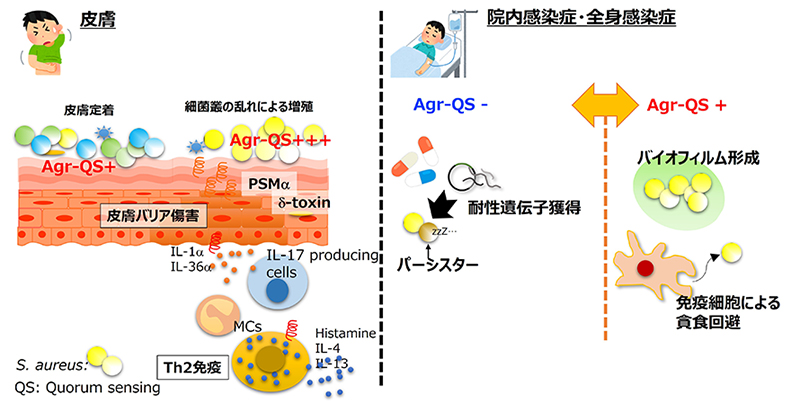
菌のクオラムセンシングと免疫相互作用による疾患病態形成
私達の研究室ではこれまでに、病原細菌がクオラムセンシングを介してどのようにアトピー性皮膚炎(Atopic dermatitis, 以下AD)に関与するのかについて研究を行ってきました。特に、ADのように、感染症に分類されない疾患において、特定の病原細菌が検出されることが単なる「疾患の結果」を見ているのか、それとも「病態の形成」に関与を見極めることが疾患の病態理解に重要です。アトピー性皮膚炎で見られるStaphylococcus aureusは皮膚上でクオラムセンシングのゲノムを変異させずに維持することで、乳児期の皮膚に生着しAD発症に関連するとともに、このクオラムセンシング領域に依存する毒素の産生を介して皮膚バリアや免疫に影響し、ADの皮膚炎を悪化させることが分かってきました。乳児期のADの発症はその後のアレルギーマーチと言われる食物アレルギーや喘息などの発症に関与することから、その皮膚における宿主免疫と微生物の相互メカニズムを解明することは重要です。現在、細菌ゲノム解析や、免疫学的な検討からこのアレルギーの発症起点に関与する未病の解析を行うとともに、これまでの病原細菌のゲノム解析技術などを用いて、院内薬剤耐性菌感染症の難治化のメカニズムなどの研究も行っています。
主任研究者
松岡 悠美 教授

研究内容
皮膚アレルギー生体防御
学歴
| 2003 | 山梨医科大学 医学部医学科卒業 |
|---|---|
| 2009 | 医学(博士) (千葉大学) |
| 2015 | 皮膚科専門医 (日本皮膚科学会)(千葉大学) |
職歴
| 2003 | 山梨大学医学部附属病院皮膚科 医員 |
|---|---|
| 2006 | 千葉大学医学部附属病院皮膚科 医員 |
| 2009 | ミシガン大学病理学教室Gabriel Nunez研究室リサーチフェロー |
| 2013 | 一般財団法人日本予防医学協会 リサーチフェロー |
| 2014 | 千葉大学大学院医学研究院 助教 |
| 2018 | 千葉大学大学院医学研究院 講師 |
| 2020 | 大阪大学免疫学フロンティア研究センター 特任准教授 |
| 2022 | 大阪大学免疫学フロンティア研究センター 准教授 |
| 2023 | 大阪大学免疫学フロンティア研究センター 教授 |
メンバー
- 松岡 悠美 教授
ymatsuokaderma.med.osaka-u.ac.jp
業績
論文
-
Nakamura Y, Kambe N, Saito M, Nishikomori R, Kim YG, Murakami M, Núñez G, Matsue H.; Mast cells mediate neutrophil recruitment and vascular leakage through the NLRP3 inflammasome in histamine-independent urticaria. J Exp Med. 2009 ; 206(5):1037-46.
-
Nakamura Y, Franchi L, Kambe N, Meng G, Strober W, Núñez G.; Critical role for mast cells in interleukin-1β-driven skin inflammation associated with an activating mutation in the nlrp3 protein. Immunity. 2012 ; 37(1):85-95.
-
Nakamura Y, Oscherwitz J, Cease KB, Chan SM, Muñoz-Planillo R, Hasegawa M, Villaruz AE, Cheung GY, McGavin MJ, Travers JB, Otto M, Inohara N, Núñez G. Staphylococcus δ-toxin induces allergic skin disease by activating mast cells. Nature. 2013 ; 503(7476):397-401.
-
Nakagawa S, Matsumoto M, Katayama Y, Oguma R, Wakabayashi S, Nygaard T, Saijo S, Inohara N, Otto M, Matsue H, Núñez G, Nakamura Y. Staphylococcus aureus Virulent PSMα Peptides Induce Keratinocyte Alarmin Release to Orchestrate IL-17-Dependent Skin Inflammation. Cell Host Microbe. 2017 ; 22(5):667-677.
-
Baldry M, Nakamura Y, Nakagawa S, Frees D, Matsue H, Núñez G, Ingmer H. Application of an agr-specific anti-virulence Compound as Therapy for Staphylococcus Aureus-induced Inflammatory Skin Disease. J Infect Dis. 2018 ; 218(6):1009-1013.
-
Miyachi H, Wakabayashi S, Sugihira T, Aoyama R, Saijo S, Koguchi-Yoshioka H, Fujimoto M, Núñez G, Matsue H, Nakamura Y. Keratinocyte IL-36 Receptor/MyD88 Signaling Mediates Malassezia-Induced IL-17-Dependent Skin Inflammation. J Infect Dis. 2021;223(10):1753-1765.
-
Nakamura Y, Takahashi H, Takaya A, Inoue Y, Katayama Y, Kusuya Y, Shoji T, Takada S, Nakagawa S, Oguma R, Saito N, Ozawa N, Nakano T, Yamaide F, Dissanayake E, Suzuki S, Villaruz A, Varadarajan S, Matsumoto M, Kobayashi T, Kono M, Sato Y, Akiyama M, Otto M, Matsue H, Núñez G, Shimojo N. Staphylococcus Agr virulence is critical for epidermal colonization and associates with atopic dermatitis development. Sci Transl Med. 2020 ; 12(551): eaay4068. doi: 10.1126/scitranslmed.aay4068.
-
Matsumoto M, Nakagawa S, Zhang L, Nakamura Y, Villaruz AE, Otto M, Wolz C, Inohara N, Núñez G. Interaction between Staphylococcus Agr virulence and neutrophils regulates pathogen expansion in the skin. Cell Host Microbe. 2021 ;29(6):930-940.
