老化生物学
Aging Biology
TEL 06-6879-4261
概要
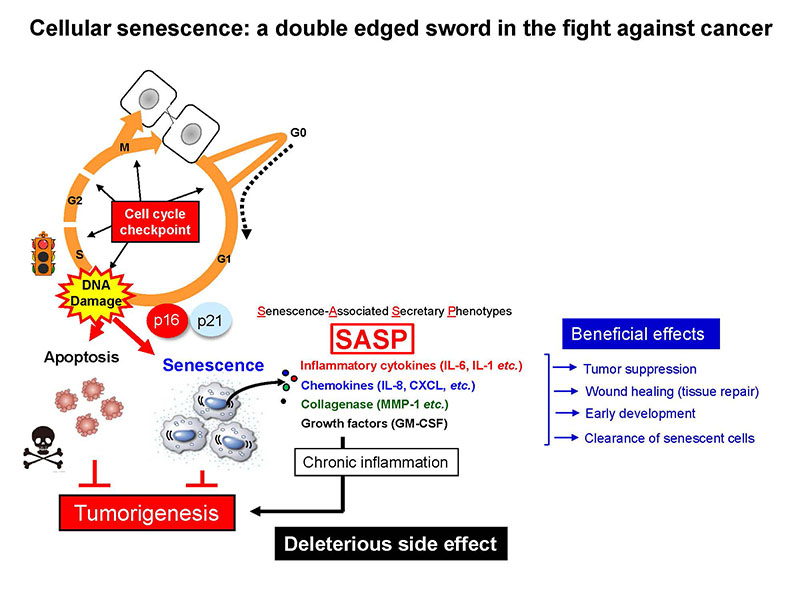
真核生物の細胞は細胞の内外から受ける様々なストレスに応答してその表現型を変化させる。特に脊椎動物の体細胞の場合、過度な細胞分裂の繰り返しやがん遺伝子の活性化など発がんの危険性があるストレスが生じると、細胞周期が不可逆的に停止することが知られている。この現象は「細胞老化」と呼ばれ、異常細胞の増殖を防ぐ重要ながん抑制機構として生体の恒常性維持に寄与していると長い間考えられてきた。しかし、近年、細胞老化を起こした細胞は単に増殖を停止しているだけではなく、炎症性サイトカイン、ケモカイン、増殖因子や細胞外マトリックス分解酵素など、炎症やがんの進展を促進する作用を有する様々な分泌因子を高発現するSASPと呼ばれる現象を起こすことが明らかになってきた。このため細胞老化は初期にはがん抑制機構として働くが、加齢に伴い、体内に老化細胞が蓄積し過ぎると、今度はSASPを介してがんを含む様々な加齢性疾患の発症を促進することが明らかになりつつある。我々の研究室では細胞老化誘導機構の解明とその制御を通して個体老化及び老化関連疾患の理解と制御を目指しています。
主任研究者
原 英二 教授

研究内容
がんと老化における細胞老化の分子機構とその役割
学歴
| 1993 | 東京理科大学大学院博士課程 修了 |
|---|
職歴
| 1993.3 | カリフォルニア大学バークレー校 ポスドク |
|---|---|
| 1995.1 | 英国王立がん研究財団研究所 ポスドク |
| 1997.1 | 京都府立医科大学 医学部 講師 |
| 1998.9 | 英国がん研究財団パータソンがん研究所 グループリーダー |
| 2003.3 | 徳島大学 ゲノム機能研究センター 教授 |
| 2008.4 | 公益財団法人がん研究会 がん研究所 部長 |
| 2015.4 | 大阪大学 微生物病研究所 教授 |
| 2015.4 | 公益財団法人がん研究会 がん研究所 部長(非常勤) |
| 2018.8 | 大阪大学 免疫学フロンティア研究センター 教授 |
受賞・表彰
| 2005 | 井上科学振興財団井上フェロー |
|---|---|
| 2012 | がん研究会学術賞 |
| 2014 | 日本癌学会 JCA-Mauvernay Award |
メンバー
- 原 英二 教授
eharabiken.osaka-u.ac.jp
業績
論文
- Takahashi, A., Loo, T. M., Okada, R., Kamachi, F., Watanabe, Y., Wakita, M., Watanabe, S., Kawamoto, S., Miyata, K., Barber, G. N., Ohtani, N. & *Hara, E. Downregulation of cytoplasmic DNases is implicated in cytoplasmic DNA accumulation and SASP in senescent cells. Nature Commun., 9: 1249 (2018).
- *Okuma, A., Hanyu, A., Watanabe, S., & *Hara, E. p16INK4a and p21Cip1/Waf1 promote tumour growth by enhancing myeloid-derived suppressor cells chemotaxis. Nature Commun., 8: 2050 (2017).
- *Takasugi, M., Okada, R., Takahashi, A., Chen, D.V., Watanabe, S., & *Hara, E. Small extracellular vesicles secreted from senescent cells promote cancer cell proliferation through EphA2. Nature Commun., 8: 15728 (2017).
- *Takahashi, A., Okada, R., Nagao, K., Kawamata, Y., Hanyu, A., Yoshimoto, S., Takasugi, M., Watanabe, S., Kanemaki, M.T., Obuse, C. & *Hara, E. Exosomes maintain cellular homeostasis by excreting harmful DNA from cells. Nature Commun., 8: 15287 (2017).
- Sato, S., Kawamata, Y., Takahashi, A., Imai, Y.,Hanyu, A., Okuma, A., Takasugi, M., Yamakoshi, K., Sorimachi, H., Kanda, H., Ishikawa, Y., Sone, S., Nishioka, Y., *Ohtani, N. & *Hara, E. Ablation of the p16INK4a tumour suppressor reverses ageing phenotypes of klotho mice. Nature Commun., 6: 7035 (2015).
- Imai, Y., Takahashi, A., Hanyu, A., Hori, S., Sato, S., Naka, K., Hirao, A., Ohtani, N. & *Hara, E. Crosstalk between the Rb Pathway and AKT Signaling Forms a Quiescence-Senescence Switch.Cell Rep., 7: 194-207 (2014)
- Yoshimoto, S., Loo, T.M., Atarashi, K., Kanda, H., Sato, S., Oyadomari, S., Iwakura, Y., Oshima, K., Morita, H., Hattori, M., Honda, K., Ishikawa, Y., *Hara, E. & Ohtani, N. Obesity-induced gut microbial metabolite promotes liver cancer through senescence secretome. Nature, 499: 97-101(2013)
- Takahashi, A., Imai, Y., Yamakoshi, K., Kuninaka, S., Ohtani, N., Yoshimoto, S., Hori, S., Tachibana, M., Anderton, E., Takeuchi, T., Shinkai, Y., Peters, G., Saya, H. & *Hara, E. DNA damage signaling triggers degradation of histone methyltransferases through APC/CCdh1 in senescent cells. Mol. Cell, 45: 123-131(2012)
- Yamakoshi, K., Takahashi, A., Hirota, F., Nakayama, R., Ishimaru, N., Kubo, Y., Mann, D.J., Ohmura, M., Hirao, A., Saya, H., Arase, S., Hayashi, Y., Nakao, K., Matsumoto, M., *Ohtani, N. & *Hara, E. Real-time in vivo imaging of p16INK4a reveals cross-talk with p53. J. Cell Biol., 186: 393-407 (2009)
- *Ohtani, N., Imamura, Y., Yamakoshi, K., Hirota, F., Nakayama, R., Kubo, Y., Ishimaru, N., Takahashi, A., Hirao, A., Shimizu, T., Mann, D.J., Saya, H., Hayashi, Y., Arase, S., Matsumoto, M., Nakao, K. & Hara, E. Visualizing the dynamics of p21Waf1/Cip1 cyclin-dependent kinase inhibitor expression in living animals Proc. Natl. Acad. Sci. USA, 104: 15034-15039 (2007)
- Takahashi, A., Ohtani, N., Yamakoshi, K., Iida, S., Tahara, H.,Nakayama, K., Nakayama, K.I., Ide, T., Saya, H. & *Hara, E. Mitogenic signalling and the p16INK4a-Rb pathway cooperate to enforce rreversible cellular senescence Nature Cell Biol., 8: 1291-1297 (2006)
- Maehara, K., Yamakoshi, K., Ohtani, N., Kubo, Y., Takahashi, A., Arase, S., Jones, N. & *Hara, E. Reduction of total E2F/DP activity induces senescence-like cell cycle arrest in cancer cells lacking functional pRB and p53. J. Cell Biol., 167: 553-560 (2005)
- Ohtani, N., Brennan, P., Gaubatz, S., Sanij, E., Hertzong, P., Wolvetang, E., Ghysdael, J., Rowe, M. & *Hara, E. Epstein-Barr virus LMP1 blocks p16 INK4a-RB-pathway by promoting nuclear export of E2F4/5. J. Cell Biol., 162: 173-183 (2003)
- Ohtani, N., Zebedee, Z., Huot, T.J.G., Stinson, J.A., Sugimoto, M., Ohashi, Y., Sharrrocks, A.D., Peters, G. & *Hara, E. Opposing effects of Ets and Id proteins on p16INK4a expression during cellular senescence. Nature, 409: 1067-1070 (2001).
- Sugimoto, M., Nakamura, T., Ohtani, N., Hampson, L., Hampson, I.N., Shimamoto, A., Furuichi, Y., Okumura, K., Niwa, S., Taya Y. & *Hara, E. Regulation of CDK4 activity by a novel CDK4 binding protein, p34SEI-1. Genes & Dev., 13: 3027-3033 (1999).
