免疫応答動態学
Immune Response Dynamics
TEL 06-6879-4939
FAX 06-6879-4938
概要
神経系による免疫制御の細胞・分子基盤の解明
神経系が免疫系の調節に関わっていることは古くから指摘されてきましたが、その仕組みは今なお十分に理解されていません。そこで我々は、神経系による免疫制御のメカニズムを細胞および分子レベルで解明することを目的として研究に取り組んでいます。これまでの我々の研究から、交感神経がリンパ球の体内動態を制御する分子機構が明らかになりました(J. Exp. Med. 2014、図1)。さらに我々は、この仕組みが免疫応答の日内変動を生み出していることも突き止めました(J. Exp. Med. 2016)。近年、神経系と免疫系の相互作用は、生命科学領域の新しい研究テーマとして注目され、世界的に活発に研究が行われています。我々の研究室では、この新しい研究分野を開拓すべく研究を進めています。
炎症性疾患の病態解明と治療法の開発
我々は、免疫細胞の動きを司るケモカイン受容体のシグナル制御因子として、copper metabolism MURR1 domain-containing (COMMD) 3とCOMMD8というタンパクから成る複合体(COMMD3/8複合体)を同定し、COMMD3/8複合体が生体内でのリンパ球の移動と免疫応答の成立に重要な役割を果たしていることを明らかにしました(J. Exp. Med. 2019、図2)。さらに、最近の我々の研究から、COMMD3/8複合体が炎症性疾患の病態に関与することも示唆されています。そこで、我々の研究室では、COMMD3/8複合体をはじめとする免疫制御因子の炎症性疾患の病態における役割を解明するとともに、それらを標的とした炎症性疾患の治療法を開発することを目標として、疾病の治療に直結する研究にも取り組んでいます。
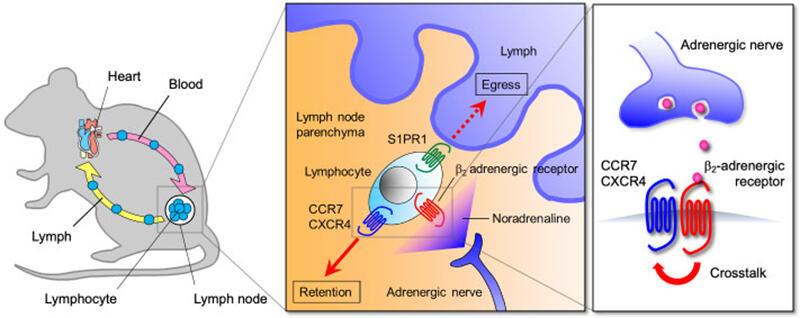
交感神経からの入力によりリンパ球のβ2アドレナリン受容体が刺激されると、リンパ球をリンパ節に保持するためのケモカイン受容体CCR7およびCXCR4の反応性が上昇する結果、リンパ球のリンパ節からの脱出が抑制される。この仕組みは、リンパ節における免疫応答の日内変動の形成にも寄与している。
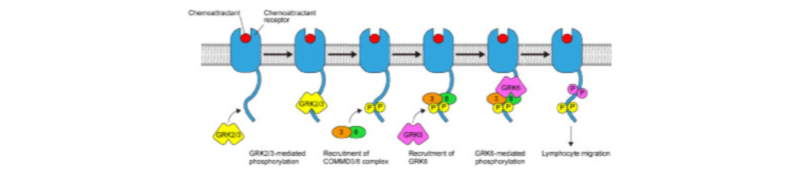
COMMD3/8複合体は、ケモカイン受容体にシグナル伝達分子GRK6を動員するアダプターとして機能し、ケモカイン受容体のシグナル伝達を促進する役割を果たしている。
主任研究者
鈴木 一博 教授

研究内容
神経系による免疫制御の細胞・分子基盤の解明
炎症性疾患の病態解明と治療法の開発
学歴
| 1998.3 | 東京大学理学部化学科 卒業 |
|---|---|
| 2003.3 | 大阪大学医学部医学科(学士編入) 卒業 |
| 2007.9 | 大阪大学大学院医学系研究科 修了(医学博士) |
職歴
| 2003.4 | 大阪大学医学部附属病院 研修医 (-2004.3) |
|---|---|
| 2006.4 | 日本学術振興会 特別研究員(DC2)(-2007.9) |
| 2007.10 | カリフォルニア大学サンフランシスコ校 博士研究員 (-2011.3) |
| 2011.4 | 大阪大学免疫学フロンティア研究センター 特任准教授 (-2017.3) |
| 2011.10 | 科学技術振興機構さきがけ研究者(兼任)(-2015.3) |
| 2017.4 | 大阪大学免疫学フロンティア研究センター 教授 |
| 2026.1 | 大阪大学大学院医学系研究科 教授 |
| 2026.1 | 大阪大学免疫学フロンティア研究センター 教授(兼任) |
受賞・表彰
| 2024 | 日本免疫学会賞(日本免疫学会) |
|---|---|
| 2016 | 日本医師会医学研究奨励賞(日本医師会) |
| 2016 | 2016 最優秀理事長賞(アステラス病態代謝研究会) |
| 2016 | 2016 優秀発表賞(アステラス病態代謝研究会 |
| 2012 | 日本免疫学会研究奨励賞(日本免疫学会) |
| 2009 | 井上研究奨励賞(井上科学振興財団) |
| 2008 | 2008 長期フェローシップ(ヒューマン・フロンティア・サイエンス・プログラム) |
| 2008 | 山村賞(大阪大学大学院医学系研究科) |
| 2003 | 山村賞(大阪大学医学部医学科) |
メンバー
- 鈴木 一博 教授
ksuzukiifrec.osaka-u.ac.jp - 白井 太一朗 助教
shiraiifrec.osaka-u.ac.jp - 小森 里美 助教
skomoriifrec.osaka-u.ac.jp - 中井 晶子 招へい教員
業績
論文
- Shirai, T., Nakai, A., Ando, E, Fujimoto, J., Leach, S., Arimori, T., Higo, D., van Eerden, F.J., Tulyeu, J., Liu, Y-C., Okuzaki, D., Murayama, M.A., Miyata, H., Nunomura, K., Lin, B., Tani, A., Kumanogoh, A., Ikawa, M., Wing, J.B., Standley, D.M., Takagi, J., Suzuki, K. Celastrol suppresses humoral immune responses and autoimmunity by targeting the COMMD3/8 complex. Sci. Immunol. 8: eadc9324, 2023.
- Nakai, A., Fujimoto, J., Miyata, H., Stumm, R., Narazaki, M., Schulz, S., Baba, Y., Kumanogoh, A. and Suzuki, K. The COMMD3/8 complex determines GRK6 specificity for chemoattractant receptors. J. Exp. Med. 216: 1630-1647, 2019.
- Suzuki, K., Hayano, Y., Nakai, A., Furuta, F. and Noda, M. Adrenergic control of the adaptive immune response by diurnal lymphocyte recirculation through lymph nodes. J. Exp. Med. 213: 2567-2574, 2016.
- Nakai, A., Hayano, Y., Furuta, F., Noda, M. and Suzuki, K. Control of lymphocyte egress from lymph nodes through β2-adrenergic receptors. J. Exp. Med. 211: 2583-2598, 2014.
- Green, J.A., Suzuki, K., Cho, B., Willison, D., Palmer, D., Allen, C.D.C., Schmidt, T.H., Xu, Y., Proia, R., Coughlin, S.R. and Cyster, J.G. The sphingosine 1-phosphate receptor S1P2 maintains the homeostasis of germinal center B cells and promotes niche confinement. Nat. Immunol. 12: 672-680, 2011.
- Suzuki, K., Grigorova, I., Phan, T.G., Kelly, L.M. and Cyster, J.G. Visualizing B cell capture of cognate antigen from follicular dendritic cells. J. Exp. Med. 206: 1485-1493, 2009
- Suzuki, K., Kumanogoh, A. and Kikutani, H. Semaphorins and their receptors in immune cell interactions. Nat. Immunol. 9: 17-23, 2008.
- Suzuki, K., Okuno, T., Yamamoto, M., Pasterkamp, R.J., Takegahara, N., Takamatsu, H., Kitao, T., Takagi, J., Rennert, P.D., Kolodkin, A.L., Kumanogoh, A. and Kikutani, H. Semaphorin 7A initiates T-cell-mediated inflammatory responses through α1β1 integrin. Nature 446: 680-684, 2007.
