ワクチン学
Vaccine Science
TEL 03-5449-5314
概要
これまで一貫して、感染症やその他免疫関連疾患における核酸(DNA, RNA)の免疫制御機構とその生理学的意義の解明、及び核酸を利用したワクチン、アジュバント、代替免疫療法開発を行っています。これらの研究成果をもとに、自身の臨床経験や治験審査の経験など最大限生かし、"Bench to Clinic"の具現化を目標にしています。
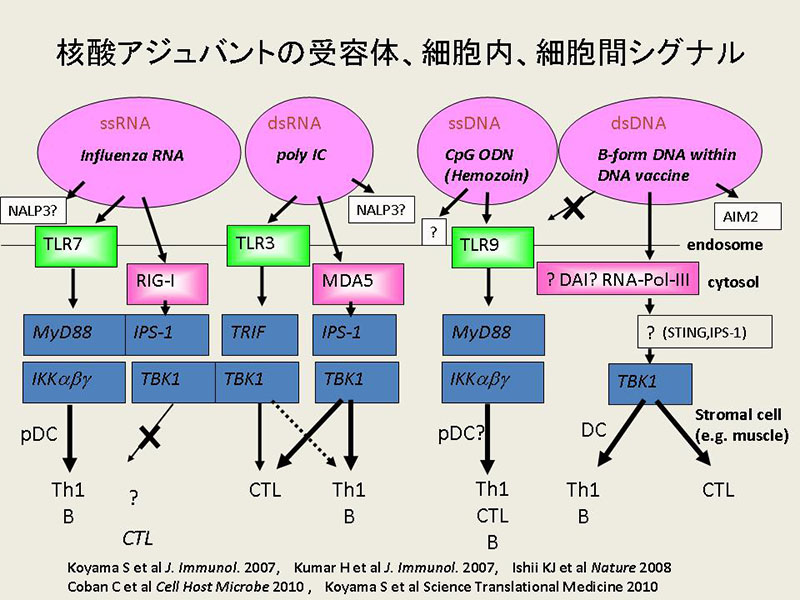
[研究項目1]「ワクチン(アジュバント)の細胞内および細胞間シグナルの分子基盤とその応用」(図1)
ワクチンは現存する医療技術の中で、その起源が最も古く、かつ最も成功したもののひとつですが、その分子レベルのでメカニズムが解明されたとはいえない状況です。そこで我々の研究グループは、過去に成功を収めた感染症ワクチンや開発が進んでいる新規ワクチン、およびアジュバントによって引き起こされる宿主の細胞内、細胞間のシグナル伝達を分子レベルで解明することを研究の目標に掲げています。
本研究は1)感染症ワクチンによって活性化される自然免疫受容体を介した細胞内、細胞間シグナル伝達(ワクチンシグナル)の分子レベルでの全容解明を目指し、さらに2)生体内レベルでのワクチンの細胞内、細胞間のトラフィック、プロセッシング、抗原提示やエフェクター機構を細胞レベルで誘導または操作可能になる技術を開発することにより、多くの感染症、各種免疫疾患にも応用可能な次世代ワクチン開発への分子基盤を形成することを目的とします。本研究により、分子メカニズムに基づいた特異性の高いワクチンやアジュバントを開発することが可能になり効果のみならず安全性の向上も期待されます。本研究は医薬基盤研究所にて主におこなわれ、当センター自然免疫学研究室(審良静男教授)との共同研究として進行中です。
[研究項目2]「ワクチン(アジュバント)受容体の構造解析」
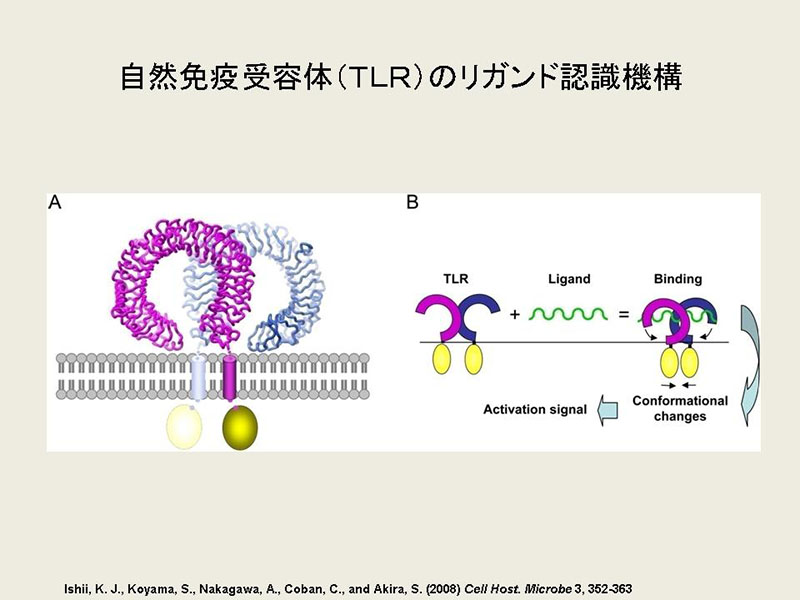
(文部科学省・タ-ゲットタンパク研究プログラム・自然免疫システムにおける病原体認識に関わる分子群の構造解析)(図2)
感染症をはじめとした各種免疫関連疾患において、いわゆる炎症反応といわれていた宿主自然免疫反応がその後の生体防御や病態形成に重要な役割を担っていることが明らかになってきました。その中でもToll様受容体や細胞内RIG受容体などは、病原体や感染宿主細胞由来の分子を特異的に認識し、それぞれ異なる細胞内シグナル分子を介して免疫システムを活性化することが知られています。本研究はこれらの自然免疫における病原体認識機構を、遺伝子欠損マウス等を用いた機能解析結果に基づき、受容体と病原体由来リガンド分子の相互作用を受容体蛋白質、及び受容体とリガンドの複合体の構造解析及び機構解析を行うことにより、3次元的な自然免疫分子認識・分子間相互作用機構を明らかにすることを目的とするものです。これらの研究によって得られた知見を基に、感染症、アレルギー、ガン、自己免疫といった免疫関連疾患に対する新たな治療法、たとえば新規アジュバントなどの免疫賦活剤、ある種の免疫反応に特異的な免疫抑制剤の開発につながることが期待されます。本研究は蛋白質研究所の中川敦史教授との共同研究です。
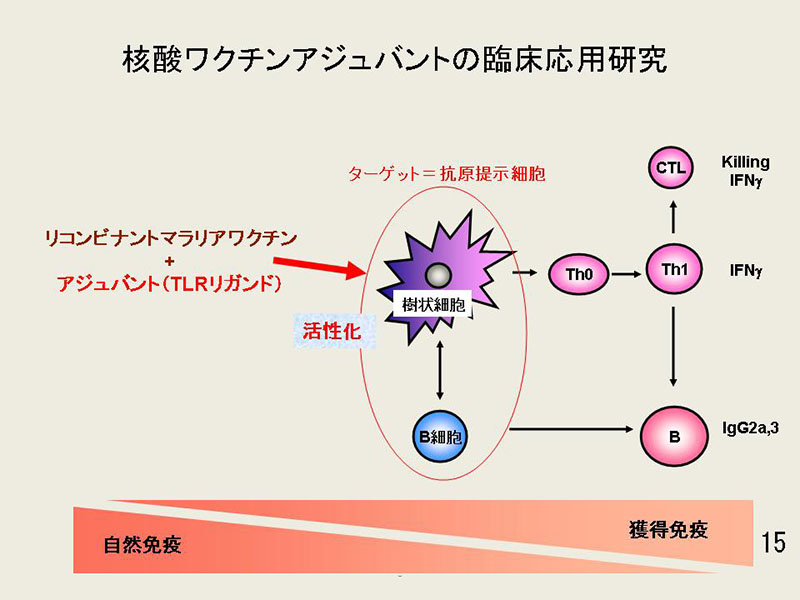
[研究項目3]「核酸ワクチンアジュバントの臨床応用研究」
(経済産業省/NEDOスーパー特区;基礎研究から臨床研究への橋渡し促進技術開発:自然免疫を刺激する次世代トラベラーズマラリアワクチンの開発)(図3)
我々は、微生物病研究所の堀井俊宏教授とともに行った研究にて、熱帯熱マラリア原虫SERAタンパク由来SE36抗原と同時に接種することにより免疫原性を著しく上昇させ、長期にわたってその上昇を維持しうるヒト型CpGODNを見いだしています。これらのCpGODNは(株)ジーンデザインにてGMP準拠の製剤化の準備を開始しています。また(財)阪大微生物病研究会は、SE36抗原をGMP下で製造する技術開発を終え、SE36抗原ワクチン試験薬作成をおこなっています。
このような背景から本研究では、SE36抗原と同時に接種することにより免疫原性を著しく向上させるアジュバントを開発するために、動物実験を通じてヒト型CpGODNの最適化を行い(研究開発項目①)、その製造技術と品質保証技術を開発(研究開発項目②)し、ヒトへの投与に向けCpGODN含有SE36抗原ワクチンの製剤化を検討します(研究開発項目③)。製剤化された新規ワクチンの探索的臨床研究を阪大医学部付属病院の未来医療センター(予定)にて行い、その安全性及び有効性を検証する(研究開発項目④)。事業化に向け、関連する技術の動向を調査し、開発した技術の占有性の確保に努める(研究開発項目⑤)。
①ヒト型CpGODNアジュバントの最適化と作用機序解析(アジュバントの研究開発)
②ヒト型CpGODNの製造技術と品質保証技術(CMC)の開発
③CpGODN含有SE36抗原ワクチンの製剤化のための研究開発
④新規ワクチン製剤の探索的臨床研究
⑤総合調査研究
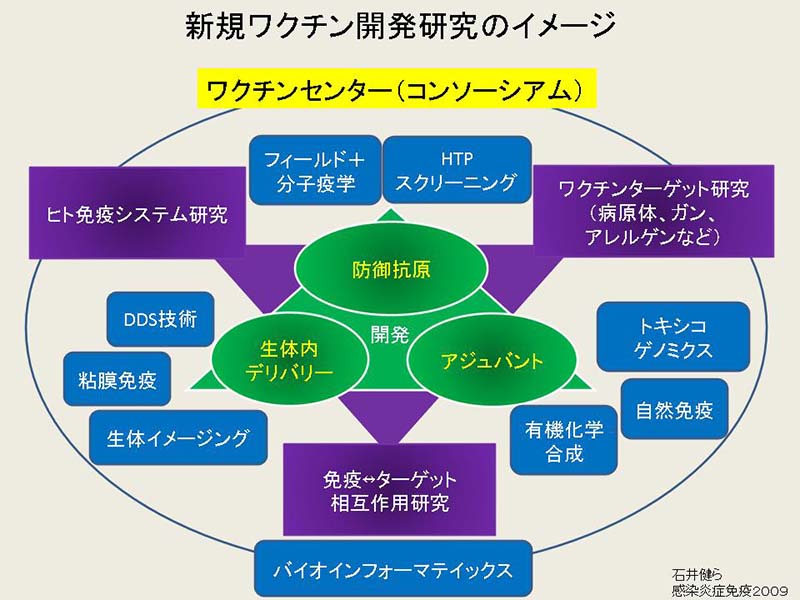
参考資料「新規ワクチン開発研究のイメージ」
主任研究者
石井 健 教授

研究内容
ワクチンの作用機序、臨床開発、審査に関する研究
学歴
| 1993.3 | 横浜市立大学医学部卒業 |
|---|
職歴
| 1993.4 | 横浜市立大学医学部付属病院研修医 |
|---|---|
| 1995.4 | 横浜市立市民病院麻酔科常勤医 |
| 1996.4 | 横浜市立大学医学部麻酔科 |
| 1996.10 | 米国保健省食品薬品局(FDA)生物学的製剤評価研究センター ワクチン部門 客員研究員 |
| 2000.3 | 米国保健省食品薬品局(FDA)生物学的製剤評価研究センター ワクチン部門 臨床試験審査官 |
| 2003.10 | 科学技術振興機構ERATO審良自然免疫プロジェクト グループリーダー |
| 2006.12 | 大阪大学微生物病研究所 難治感染症対策研究センター 分子原虫学分野 准教授 |
| 2007.12 | 大阪大学免疫学フロンテイア研究センター 准教授 (兼任) |
| 2008.8 | 文部科学省 研究振興局 学術調査官 (非常勤) |
| 2010.4 | 医薬基盤研究所 プロジェクトリーダー |
| 2010.4 | 大阪大学免疫学フロンティア研究センター ワクチン学 教授 |
| 2015.4 | 医薬基盤・健康・栄養研究所 ディレクター |
| 2019 | 大阪大学免疫学フロンティア研究センター 招へい教授 |
| 2019 | 東京大学医科学研究所 教授 |
受賞・表彰
| 2019 | 22nd JSI Award |
|---|---|
| 2014 | 32th Osaka Science Prize |
| 2014 | ‘Highly cited researcher’ in Thomson Reuters THE WORLD'S MOST INFLUENTIAL SCIENTIFIC MINDS 2014 |
| 2012 | Thinking inside the box award DNA vaccines |
| 2010 | Isamu Tagaya Memorial Vaccine Research Award |
| 2008 | Japanese Society of Immunology, Young Investigator Award |
| 2007 | ‘Rising star in Immunology’(Sep 2007) Thompson Reuter’s ISI |
メンバー
-
石井 健 教授
kenishiiims.u-tokyo.ac.jp (東京大学医科学研究所)
業績
論文
- Temizoz B, Kuroda E, Ohata K, Jonai N, Ozasa K, Kobiyama K, Aoshi T, Ishii KJ*. TLR9 and STING agonists synergistically induce innate and adaptive type II IFN. Eur J Immunol. 2015. 45(4) 1159?1169
- Onishi M, Ozasa K, Kobiyama K, Ohata K, Kitano M, Taniguchi K, Homma T, Kobayashi M, Sato A, Katakai Y, Yasutomi Y, Wijaya E, Igarashi Y, Nakatsu N, Ise W, Inoue T, Yamada H, Vandenbon A, Standley DM, Kurosaki T, Coban C, Aoshi T, Kuroda E, Ishii KJ* Hydroxypropyl-β-Cyclodextrin Spikes Local Inflammation That Induces Th2 Cell and T Follicular Helper Cell Responses to the Coadministered Antigen. J Immunol. 2015 194(6):2673-82.
- Koo CX, Kobiyama K, Shen YJ, LeBert N, Ahmad S, Khatoo M, Aoshi T, Gasser S, Ishii KJ*. RNA Polymerase III Regulates Cytosolic RNA:DNA Hybrids and Intracellular MicroRNA Expression. J Biol Chem. 2015. 290(12):7463-73
- Onishi M, Kitano M, Taniguchi K, Homma T, Kobayashi M, Sato A, Coban C, Ishii KJ* Hemozoin is a potent adjuvant for hemagglutinin split vaccine without pyrogenicity in ferrets Vaccine 2014 32(25):3004-9.
- Kobiyama K, Aoshi T, Narita H, Kuroda E, Hayashi M, Tetsutani K, Koyama S, Mochizuki S, Sakurai K, Katakai Y, Yasutomi Y, Saijo S, Iwakura Y, Akira S, Coban C, Ishii KJ*. Nonagonistic Dectin-1 ligand transforms CpG into a multitask nanoparticulate TLR9 agonist. Proc Natl Acad Sci U S A. 2014 111(8):3086-91. (Direct submission)
- Kobiyama K, Kawashima A, Jounai N, Takeshita F, Ishii KJ, Ito T, Suzuki K. Role of Extrachromosomal Histone H2B on Recognition of DNA Viruses and Cell Damage. Front Genet. 2013 4:91.
- Tang CK, Aoshi T, Jounai N, Ito J, Ohata K, Kobiyama K, Dessailly BH, Kuroda E, Akira S, Mizuguchi K, Coban C, Ishii KJ*. The chemotherapeutic agent DMXAA as a unique IRF3-dependent type-2 vaccine adjuvant. PLoS One. 2013;8(3):e60038.
- Kuroda E, Coban C, Ishii KJ* Particulate adjuvant and innate immunity:past achievements, present findings and future prospects. Int. Rev. Immunol. 2013 2013;32(2):209-20
- Jounai N, Kobiyama K, Takeshita F, Ishii KJ*. Recognition of damage-associated molecular patterns related to nucleic acids during inflammation and vaccination. Front Cell Infect Microbiol. 2012 2 (168) 1-13.
- Tetsutani K, Ishii KJ*. Adjuvants in influenza vaccines. Vaccine. 2012 30(52):7658-61.
- Desmet CJ, Ishii KJ*. Nucleic acid sensing at the interface between innate and adaptive immunity in vaccination. Nat Rev Immunol. 2012 12(7):479-91.
- Marichal T, Ohata K, Bedoret D, Mesnil C, Sabatel C, Kobiyama K, Lekeux P, Coban C, Akira S, Ishii KJ*, Bureau F*, Desmet CJ*. DNA released from dying host cells mediates aluminum adjuvant activity. Nat Med. 2011 17(8):996-1002.
- Koyama S, Aoshi T, Tanimoto T, Kumagai Y, Kobiyama K, Tougan T, Sakurai K, Coban C, Horii T, Akira S*, Ishii KJ*. Plasmacytoid dendritic cells delineate immunogenicity of influenza vaccine subtypes. Sci Transl Med. 2010 2(25):25ra24.
- Koyama S, Coban C, Aoshi T, Horii T, Akira S, Ishii KJ*. “Innate immune control of nucleic acid-based vaccine immunogenicity.” Expert Rev Vaccines. 2009 8(8):1099-107.
- Ishii KJ*, Akira S*. “Potential link between the immune system and metabolism of nucleic acids.” Curr Opin Immunol. 2008 20(5):524-9.
- Takeshita F, Ishii KJ*. “Intracellular DNA sensors in immunity.” Curr Opin Immunol. 2008 20(4):383-8
- Ishii KJ*, Koyama S, Nakagawa A, Coban C, Akira S. “Host innate immune receptors and beyond: making sense of microbial infections.” Cell Host Microbe. 2008 3(6):352-63.
- Coban C, Koyama S, Takeshita F, Akira S, Ishii KJ*. “Molecular and cellular mechanisms of DNA vaccines.” Hum Vaccin. 2008 4(6).
- Ishii KJ*, Kawagoe T, Koyama S, Matsui K, Kumar H, Kawai T, Uematsu S, Takeuchi O, Takeshita F, Coban C, Akira S*. “TANK-binding kinase-1 delineates innate and adaptive immune responses to DNA vaccines.” Nature. 2008 451(7179):725-9.
- Ishii KJ*, Akira S. “Toll or Toll-Free Adjuvant Path Toward the Optimal Vaccine Development.” J Clin Immunol. 2007 27(4):363-71.
- Ishii KJ, Uematsu S, Akira S. “’Toll' gates for future immunotherapy.” Curr Pharm Des. 2006;12(32):4135-42.
- Ishii KJ, Akira S. “Innate immune recognition of, and regulation by, DNA.” Trends Immunol. 2006 27(11):525-32.
- Ishii KJ, Coban C, Akira S. “Manifold Mechanisms of Toll-Like Receptor-Ligand recognition.” J Clin Immunol. 2005 25(6):511-521.
- Ishii KJ, Coban C, Kato H, Takahashi K, Torii Y, Takeshita F, Ludwig H, Sutter G, Suzuki K, Hemmi H, Sato S, Yamamoto M, Uematsu S, Kawai T, Takeuchi O, Akira S. “A Toll-like receptor-independent antiviral response induced by double-stranded B-form DNA.” Nat Immunol. 2006 7(1):40-48.
- Ishii KJ, Akira S.“TLR ignores methylated RNA?” Immunity. 2005 23(2):111-3.
- Ishii KJ, Akira S. “Innate immune recognition of nucleic acids: Beyond toll-like receptors.” Int J Cancer. 2005 117(4):517-23.
- Ishii KJ, Ito S, Tamura T, Hemmi H, Conover J, Ozato K, Akira S, Klinman DM. “CpG-activated Thy1.2(+) dendritic cells protect against lethal Listeria monocytogenes infection.” Eur J Immunol. 2005 35(8):2397-405.
- Ishii KJ, Gursel I, Gursel M and Klinman DM. “ Immunotherapeutic Utility of Stimulatory and Suppressive Oligonucleotides” Curr. Opin. Mol. Ther. 6(2):166-74, 2004.
- Ishii KJ*, Kawakami K, Gursel I, Klinman DM and Puri RK. “Anti-tumor therapy with bacterial DNA and toxin: Liposomal CpG ODN plus IL-13 cytotoxin induces complete regression of established human tumor in animal models.” Clinical Cancer Research. 9(17): 6516-22, 2003.
- Ishii KJ, Takeshita F, Gursel I, Gursel M, Nussenzweig A and Klinman DM. "Potential Role of PI3 Kinases, rather than DNA-PK, in CpG DNA Induced Immune Activation" J. Exp. Med. Jul 15;196(2):269-74, 2002.
- Ishii KJ, Suzuki K, Itoh Y, Coban C, Takeshita F, Matoba H, Kohn LD, Klinman DM. “Genomic DNA released by dying cells induces the maturation of antigen presenting cells.” J. Immunol. 167(5): 2602-2607, 2001.
- Klinman DM, Verthelyi D, Takeshita F, Ishii KJ. “Immune recognition of foreign DNA.” Immunity, Vol.11, 123 129, 1999.
Ishii KJ, Weiss WR, Ichino M, Verthelyi D, Hoffman SL, Klinman DM. “Activity and Safety of DNA Plasmids Encoding IL 4 and IFN gamma.” Gene Ther. 6: (2) 237 244, 1999. - Ishii KJ, Weiss WR, Klinman DM. “Prevention of neonatal tolerance by plasmid DNA encoding GMCSF.” Vaccine, Vol.18, 703-10, 1999.
著書
Ishii KJ and Tang CK (Editor in chief) “Biological DNA Sensor: The Impact of Nucleic Acids on Diseases and Vaccinology” ELSEVIER, 2013
"Nucleic Acids in Innate Immunity" Edited by Ishii KJ and Akira S, CRC press, 2008.
