自然免疫学
Host Defense
TEL 06-6879-4955
FAX 06-6879-4264
概要
自然免疫とは、細菌や原虫、ウイルスなど幅広い病原体を認識するパターン認識受容体群によって始動され、炎症反応や獲得免疫応答へと誘導する、我々の身体が生まれながらにして(自然)備え持つ防御システム(免疫)です。自然免疫学分野では、自然免疫応答を構成する遺伝子群を研究対象として、自然免疫の分子メカニズムを生体レベルで包括的に理解する研究を展開しています。
免疫応答とmRNA安定性管理機構の関係性を探る
研究室では、種々の病原体を感知するパターン認識受容体と、その活性化と細胞応答を導く一連のシグナル伝達因子の機能を解明し、自然免疫応答の全貌の理解を目指して解析を行っています。その中でパターン認識受容体の一つであるToll-like receptor(TLR)が誘導するシグナル伝達系の解析から、「mRNAの安定性」を司るRNA分解酵素Regnase-1が炎症反応を制御する新規分子メカニズムを明らかにしました。
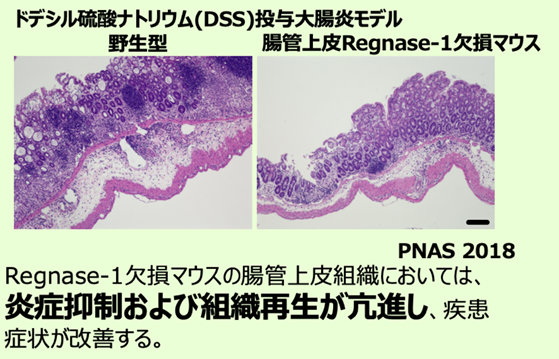
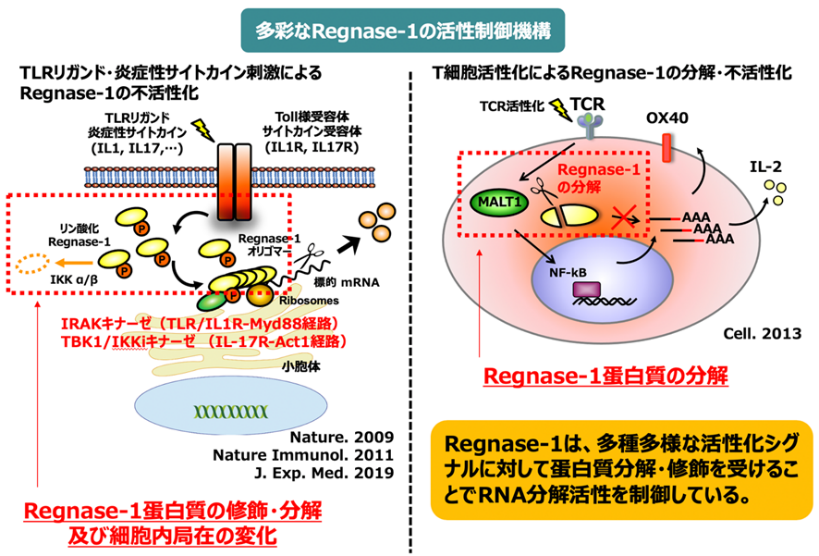
Regnase-1は自身の配列中にRNA分解活性ドメインとRNA結合モチーフを有し、そのRNA分解活性によって炎症性サイトカインのmRNAを認識・分解することで炎症反応を抑制しています。一方でTLRシグナル伝達経路が活性化されると、炎症性サイトカインmRNAの合成が速やかに促進されるとともにRegnase-1は一時的に不活性化されます。その結果、炎症性サイトカインmRNAが安定化し、炎症反応が誘導されます。つまり、通常の自然免疫担当細胞では内在性Regnase-1の作用によって極力炎症性サイトカインのmRNAは分解されている状態に保たれているのですが、ひとたび病原体侵入などの緊急時にはRegnase-1を介した抑制機構が解除され、迅速に炎症反応を促進するのです。
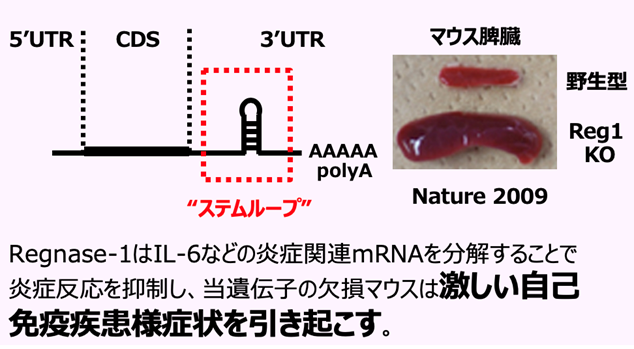
このようなRegnase-1の制御の解除メカニズムは他の炎症性刺激やT細胞の活性化でも存在することが判明しており、Regnase-1が幅広い炎症反応・細胞活性化の制御に関与していることが明らかとなっております。さらに、Regnase-1には炎症・細胞活性化以外にも細胞・臓器の機能維持ための様々な制御機構が存在することが分かってきました。これらの活性化制御機構を理解していくために、免疫細胞のみならず非免疫系細胞にも注目し、RNA代謝や免疫代謝の観点からも解析を進めています。
主任研究者
審良 静男 教授

研究内容
自然免疫による病原体認識機構
学歴
| 1977 | 大阪大学医学部卒業 |
|---|---|
| 1984 | 大阪大学医学研究科博士課程修了 |
職歴
| 1978 | 堺市立病院内科医師 |
|---|---|
| 1984 | 日本学術振興会奨励研究員 |
| 1985 | カリフォルニア大学バークレー校博士研究員 |
| 1987 | 大阪大学細胞工学センター助手(免疫研究部門) |
| 1995 | 大阪大学細胞生体工学センター助教授 |
| 1996 | 兵庫医科大学生化学教授 |
| 1999 | 大阪大学微生物病研究所教授 |
| 2007 | 大阪大学免疫学フロンティア研究センター拠点長(-2019.6) |
| 2018 | 大阪大学免疫学フロンティア研究センター 特任教授 |
受賞・表彰
| 2026 | 日本国際賞 |
|---|---|
| 2012 | フレデリックバンアワード(IEIIS) |
| 2011 | ガードナー国際賞 |
| 2011 | 吹田市長賞 |
| 2010 | 慶應医学賞 |
| 2010 | アベリー・ランドスタイナー賞(ドイツ免疫学会) |
| 2009 | 文化功労者・顕彰 |
| 2007 | ミルシュタイン賞(ICIS) |
| 2007 | 恩賜賞・日本学士院賞 |
| 2007 | 上原賞 |
| 2007 | リサーチフロントアワード(トムソン・ロイター) |
| 2006 | ウィリアム・コーリー賞(米国がん研究所) |
| 2006 | 朝日賞 |
| 2005 | 紫綬褒章 |
| 2004 | ロベルト・コッホ賞(ドイツ・コッホ財団) |
| 2004 | 高松宮妃癌研究基金学術賞 |
| 2003 | 武田医学賞 |
| 2002 | 大阪科学賞 |
| 2001 | 野口英世記念医学賞 |
| 2000 | 井上学術賞 |
メンバー
-
審良 静男 教授
sakirabiken.osaka-u.ac.jp - 前田 和彦 准教授
kazmaedabiken.osaka-u.ac.jp - 村田 暁彦 助教
amurataifrec.osaka-u.ac.jp - Arthur Millius 助教
arthur.milliusifrec.osaka-u.ac.jp
業績
論文
- Kozaki T, Komano J, Kanbayashi D, Takahama M, Misawa T, Satoh T, Takeuchi O, Kawai T, Shimizu S, Matsuura Y, Akira S, Saitoh T. Mitochondrial damage elicits a TCDD-inducible poly(ADP-ribose) polymerase-mediated antiviral response. Proc Natl Acad Sci U S A. 114(10): 2681-2686 (2017)
- Satoh T, Nakagawa K, Sugihara F, Kuwahara R, Ashihara M, Yamane F, Minowa Y, Fukushima K, Ebina I, Yoshioka Y, Kumanogoh A, Akira S. Identification of an atypical monocyte and committed progenitor involved in fibrosis. Nature. 541(7635):96-101 (2017)
- Satoh T, Akira S. Toll-Like Receptor Signaling and Its Inducible Proteins. Microbiol Spectr. 6, 4 (2016)
- Maeda K, Akira S. TLR7 Structure: Cut in Z-Loop. Immunity. 45(4):705-707 (2016)
- Martino MM, Maruyama K, Kuhn GA, Satoh T, Takeuchi O, Muller R, Akira S. Inhibition of IL-1R1/MyD88 signalling promotes mesenchymal stem cell-driven tissue regeneration. Nature Communications. 7:11051 (2016)
- Kuniyoshi K, Takeuchi O, Pandey S, Satoh T, Iwasaki H, Akira S, Kawai T. Pivotal role of RNA-binding E3 ubiquitin ligase mEX3C in RIG-I-mediated antiviral innate immunity. Proc Natl Acad Sci U S A. 111(15):5646-5651 (2014)
- Lee H, Komano J, Saitoh Y, Yamaoka S, Kozaki T, Misawa T, Takahama M, Satoh T, Takeuchi O, Yamamoto N, Matsuura Y, Saitoh T, Akira S. Zinc-finger antiviral protein mediates retinoic acid inducible gene I-like receptor-independent antiviral response to murine leukemia virus. Proc Natl Acad Sci U S A. 110(30):12379-12384 (2013)
- Uehata T, Iwasaki H, Vandenbon A, Matsushita K, Hernandez-Cuellar E, Kuniyoshi K, Satoh T, Mino T, Suzuki Y, Standley DM, Tsujimura T, Rakugi H, Isaka Y, Takeuchi O, Akira S. Malt1-Induced Cleavage of Regnase-1 in CD4+ Helper T Cells Regulates Immune Activation. Cell. 153(5):1036-1049 (2013)
- Zou J, Kawai T, Tsuchida T, Kozaki T, Tanaka H, Shin KS, Kumar H, Akira S. Poly IC Triggers a Cathepsin D- and IPS-1-Dependent Pathway to Enhance Cytokine Production and Mediate Dendritic Cell Necroptosis. Immunity. 38(49):717-728 (2013)
- Satoh T, Kidoya H, Naito H, Yamamoto M, Takemura N, Nakagawa K, Yoshioka Y, Morii E, Takakura N, Takeuchi O, Akira S. Critical role of Trib1 in differentiation of tissue-resident M2-like macrophages. Nature. 495(7442):524-528 (2013)
- Misawa T, Takahama M, Kozaki T, LeeH, Zou J, Saitoh T, Akira S. Microtubule-driven spatial arrangement of mitochondria promotes activation of the NLRP3 inflammasome. Nat Immunol. 14(5):454-460 (2013)
- Iwasaki H, Takeuchi O, Teraguchi S, Matsushita K, Uehata T, Kuniyoshi K, Satoh T, Saitoh T, Matsushita M, Standley DM, Akira S. The IκB kinase complex regulates the stability of cytokine-encoding mRNA induced by TLR-IL-1R by controlling degradation of regnase-1. Nat Immunol. 12(12):1167-1175 (2011)
- Saitoh T, Satoh T, Yamamoto N, Uematsu S, Takeuchi O, Kawai T, Akira S. Antiviral Protein Viperin Promotes Toll-like Receptor 7- and Toll-like Receptor 9-Mediated Type I Interferon Production in Plasmacytoid Dendritic Cells. Immunity. 34(3):352-63 (2011)
- Tsuchida T, Zou J, Saitoh T, Kumar H, Abe T, Matsuura Y, Kawai T, Akira S. The Ubiquitin Ligase TRIM56 Regulates Innate Immune Responses to Intracellular Double-Stranded DNA. Immunity. 33(5):765-776 (2010)
- Satoh T, Takeuchi O, Vandenbon A, Yasuda K, Tanaka Y, Kumagai Y, Miyake T, Matsushita K, Okazaki T, Saitoh T, Honma K, Matsuyama T, Yui K, Tsujimura T, Standley DM, Nakanishi K, Nakai K, Akira S. The Jmjd3-Irf4 axis regulates M2 macrophage polarization and host responses against helminth infection. Nat Immunol. 11(10):936-944 (2010)
- Satoh T, Kato H, Kumagai Y, Yoneyama M, Sato S, Matsushita K, Tsujimura T, Fujita T, Akira S, Takeuchi O. LGP2 is a positive regulator of RIG-I- and MDA5-mediated antiviral responses. Proc Natl Acad Sci U S A. 107(4):1512-1517 (2010)
- Saitoh T, Fujita N, Hayashi T, Takahara K, Satoh T, Lee H, Matsunaga K, Kageyama S, Omori H, Noda T, Yamamoto N, Kawai T, Ishii K, Takeuchi O, Yoshimori T, Akira S. Atg9a controls dsDNA-driven dynamic translocation of STING and the innate immune response. Proc Natl Acad Sci U S A. 106(49):20842-20846 (2009)
- Kawagoe T, Takeuchi O, Takabatake Y, Kato H, Isaka Y, Tsujimura T, Akira S. TANK is a negative regulator of Toll-like receptor signaling and is critical for the prevention of autoimmune nephritis. Nat Immunol. 10(9):965-972 (2009)
- Matsushita K, Takeuchi O, Standley DM, Kumagai Y, Kawagoe T, Miyake T, Satoh T, Kato H, Tsujimura T, Nakamura H, Akira S. Zc3h12a is an RNase essential for controlling immune responses by regulating mRNA decay. Nature. 458(7242):1185-1190 (2009)
- Saitoh T, Fujita N, Jang MH, Uematsu S, Yang BG, Satoh T, Omori H, Noda T, Yamamoto N, Komatsu M, Tanaka K, Kawai T, Tsujimura T, Takeuchi O, Yoshimori T, Akira S. Loss of the autophagy protein Atg16L1 enhances endotoxin-induced IL-1beta production. Nature. 456(7219):264-268 (2008)
