News & Topics
Research
2021.10.12
ヒト Xkr8-Basigin 複合体の立体構造解析(長田 G が Nat Struct Mol Biol に掲載)
PRESS RELEASE
細胞膜に局在する Xkr8-Basigin (BSG) 複合体は、一定条件下で活性化されるスクランブラーゼであり、リン脂質を非特異的に外層から内層へ、あるいは内層から外層へ双方向に移層します。IFReC免疫・生化学研究室の櫻木崇晴特任助教、長田重一特任教授らのチームは、クライオ電子顕微鏡とX線結晶構造解析を組み合わせて、3.8Åの分解能でヒト Xkr8-BSG 複合体の構造を決定しました。この構造モデルから、リン脂質スクランブルの分子メカニズムが明らかになりました。
 本論文の概念図
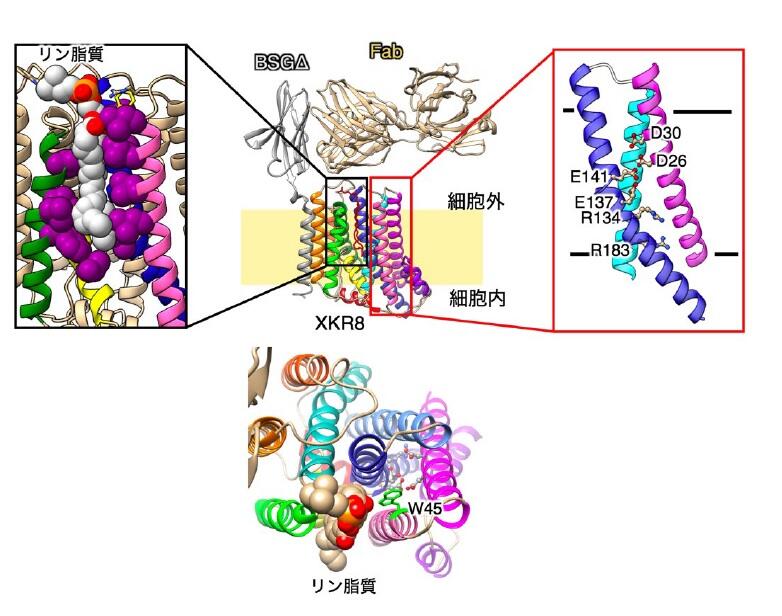
本論文の概念図
本研究で決定されたヒトXkr8-BSG-Fab複合体の立体構造。(左)Xkr8に結合したPtdChoとその周囲を囲む疎水性残基(マゼンタ)。(右)リン脂質スクランブリングに必須な荷電アミノ酸がXkr8の膜貫通領域に階段上に並んでいる。(下) 細胞外から見たXkr8分子。gatekeeper として作用するTrp残基(緑)がリン脂質とリン脂質通過領域(ポア)の境界に存在する。
解説 (PDF)
Article (外部リンク)
Contact:

長田重一(免疫・生化学)
![]() 06-6879-4953
06-6879-4953![]() snagataifrec.osaka-u.ac.jp
snagataifrec.osaka-u.ac.jp
